Die Herausforderung
Ein Pharmaunternehmen, das eine Phase-II-Studie zu einem Immuntherapeutikum für metastasierten Prostatakrebs durchführte, suchte die Unterstützung von Quibim, um Daten aus der Basis-Bildgebung zu extrahieren und zu analysieren. Da das untersuchte Medikament an das prostataspezifische Membranantigen (PSMA) bindet, wurde angenommen, dass seine Wirksamkeit mit der PSMA-Expression korreliert, wie dies in Studien zu anderen PSMA-zielenden Verbindungen festgestellt wurde1.
Das Unternehmen wollte quantitative Nachweise zur Unterstützung der Entwicklung von Screening-Protokollen für eine nachfolgende zentrale Studie, deren Ziel darin bestand, die Präzision der Patientenstratifizierung zu verbessern und die Eignungskriterien zu verfeinern, um die Studienergebnisse zu optimieren.
Die Lösung
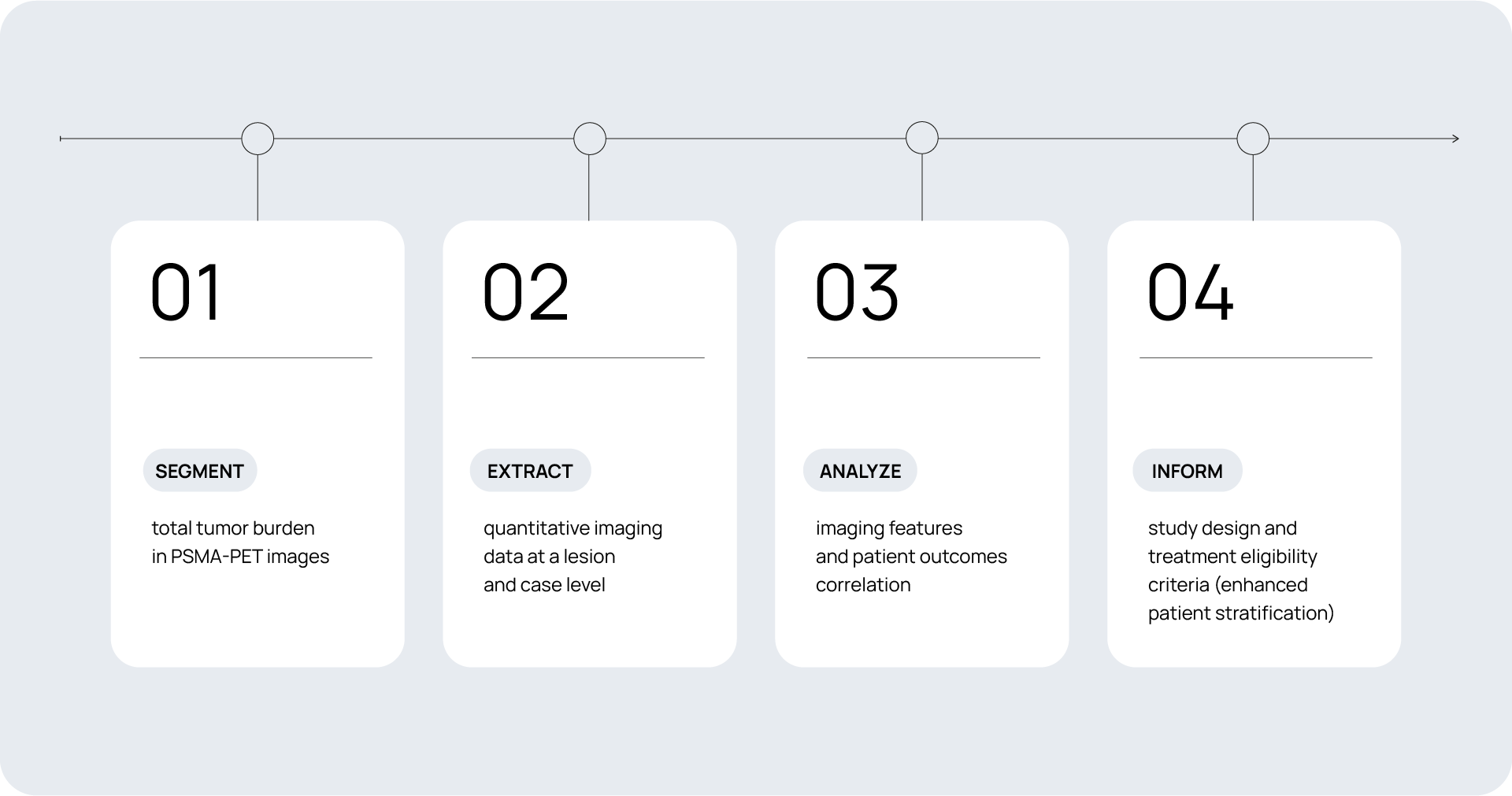
Quibim entwickelte eine Methode zur Segmentierung von Läsionen von PSMA-PET/CT-Basisbildern, zur Extraktion von über einhundert Merkmalen auf Läsions- und Fallebene pro Patient und zur Korrelation von Basisbildmerkmalen mit Behandlungsreaktion und Krankheitsverlaufswerten wie PSA-Kinetik und Zeit bis zur Progression (TTP).2Weitere Informationen zu diesem Ansatz finden Sie in unserem Blog-Artikel Von Bildern zu Erkenntnissen: Quantitatives PSMA-PET gekoppelt mit KI in klinischen Studien zu Prostatakrebs.
Das Ergebnis
Dieser Ansatz ermöglicht:
- Die Bewertung im Rahmen einer zentralen Studie, ob PSMA-PET ein geeigneter bildgebender Test für das Patientenscreening und die Stratifizierung ist.
- Die Bestimmung, welches Merkmal oder welche Merkmalskombination als bildgebender Biomarker fungieren kann, der die Reaktion auf die Behandlung, wie z. B. das radiologische progressionsfreie Überleben, genau vorhersagt. 3
- Die Identifizierung der Schwellenwerte für die Einschlusskriterien basierend auf dem Bildgebungs-Biomarker bei Erzielung eines Gleichgewichts zwischen Kriterien, die streng genug sind, um die Patientensicherheit und die Gültigkeit der Studie zu gewährleisten, jedoch nicht so restriktiv, dass sie die Rekrutierung einschränken oder die Studienpopulation nicht repräsentativ machen.
- Die Definition eines bildgebenden Biomarkers auf der Grundlage behördlich zugelassener bildgebender Verfahren, um die Generalisierbarkeit der Studie auf eine breitere Population in der klinischen Praxis zu unterstützen.
Referenzen
-
E. Delpassand et al., „Preliminary efficacy and safety results from the TATCIST trial: A PSMA-directed targeted alpha therapy with FPI-2265 (225Ac-PSMA-I&T) for the treatment of metastatic castration-resistant prostate cancer” “, präsentiert bei AACR, San Diego (CA, USA), 5.-10. April 2024, Posterpräsentation, Abstract CT224.. [Online]. Verfügbar unter: https://fusionpharma.com/wp-content/uploads/2024/04/AACR-2024-TATCIST-Study-Poster_040524_corrected.pdf
-
S. Vizel, „From images to insights: Quantitative PSMA-PET coupled with AI in prostate cancer clinical trials“. Quibim (31. Mai 2024). [Online]. Verfügbar unter: https://quibim.com/news/from-images-to-insights-quantitative-psma-pet-coupled-with-ai-in-prostate-cancer-clinical-trialspsma/
-
deSouza, NM, Achten, E., Alberich-Bayarri, A et al. „Validated imaging biomarkers as decision-making tools in clinical trials and routine practice: current status and recommendations from the EIBALL* subcommittee of the European Society of Radiology“ Insights Imaging 10, 87 (2019). https://doi.org/10.1186/s13244-019-0764-0
